Bạn đã bao giờ tự hỏi liệu chúng ta có thể điều chế natri cacbonat – một chất hóa học quan trọng – trong phòng thí nghiệm không? Hãy cùng oshivietnam.org tìm hiểu cách chế tạo natri cacbonat và khám phá ứng dụng của nó trong cuộc sống hàng ngày của chúng ta!
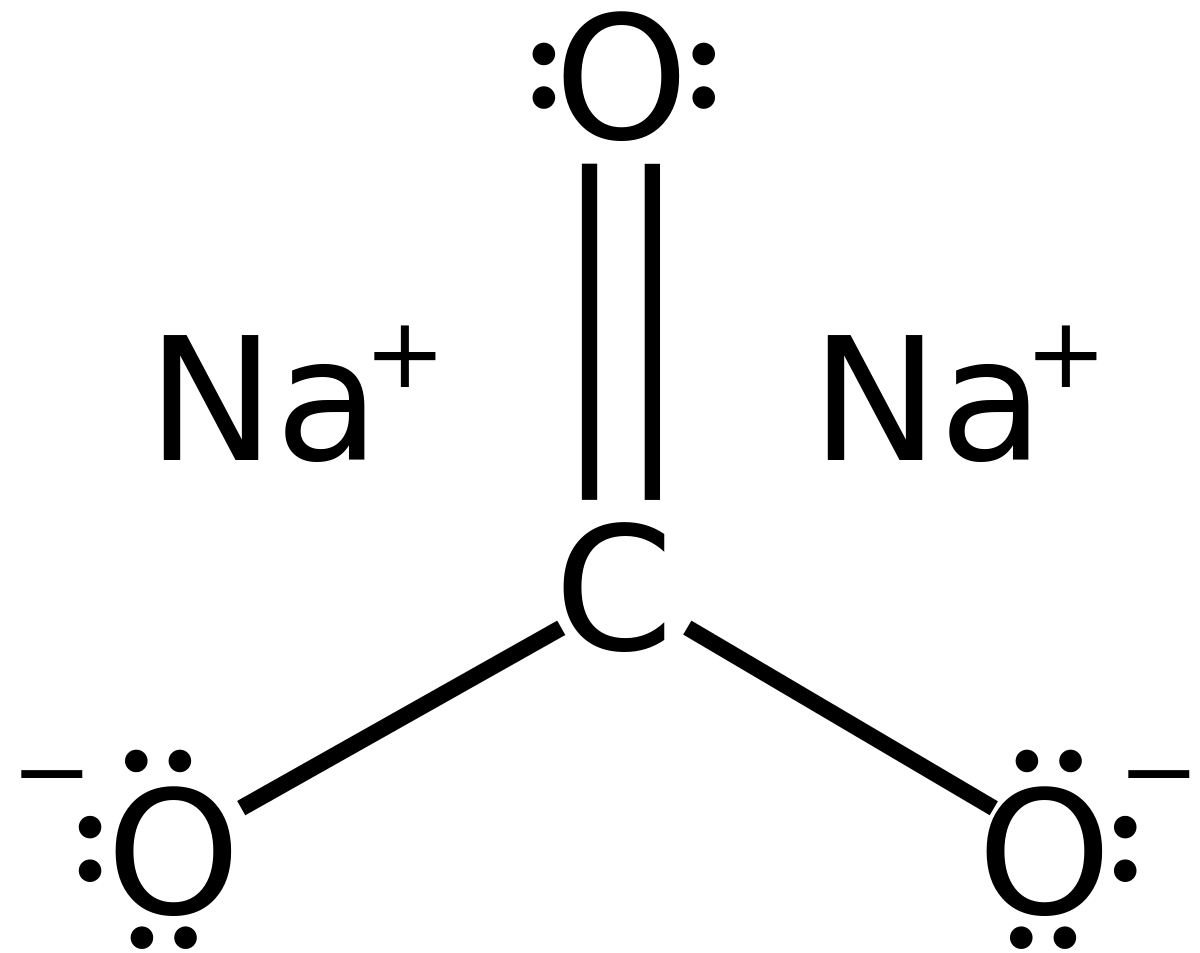
Natri Cacbonat là chất gì?
Natri cacbonat được gọi bằng tên thân thuộc là soda. Đây là một loại muối cacbonat của natri có tính chất ăn mòn cao và không được sử dụng trong thực phẩm.
Bạn đang xem: Điều Chế Natri Cacbonat – Khám Phá Cách Làm Tại Nhà!
Natri cacbonat công thức là Na2CO3.
Trong tự nhiên, Na2CO3 có thể được tìm thấy trong nước biển, nước khoáng, tro rong biển và muối mỏ trong lòng đất.
Tính chất vật lý của Na2CO3
| Trạng thái tồn tại | Chất rắn khan, không mùi, màu trắng và là một chất hút ẩm tốt. |
| Khối lượng riêng của Na2CO3 | 2.532 g/cm3, thể rắn |
| Khối lượng mol | 105.9884 g/mol |
| Nhiệt độ nóng chảy | 851oC (1124 K) |
| Nhiệt độ sôi | 1600 °C (2451 K) |
| Nhiệt độ phân hủy | 853oC |
| Độ tan | Tan hoàn toàn trong nước nóng, glycerol, axit sunfuic . Ở 20°C, độ tan trong nước là 22 g/100 ml, phản ứng tỏa nhiệt lớn. Hòa tan một phần trong dung dịch acetone, alcohol, methanol |
| Trạng thái dung dịch |
|
| Tính ăn mòn | Không ăn mòn thủy tinh nhưng dung dịch natri cacbonat đặc nóng có thể ăn mòn thép |
| Trong không khí, decahiđrat Na2CO3.10H2O dễ xảy ra hiện tượng thoát nước để trở thành dạng bột có màu trắng Na2CO3.5H2O | |

Tính chất hoá học
Gây thay đổi màu sắc của chất chỉ thị khi thủy phân trong nước, tạo ra dung dịch Na2CO3 có tính bazơ yếu: Dung dịch phenolphtalein không màu chuyển sang màu hồng.
Quỳ tím chuyển sang màu xanh.
- Na2CO3 → 2Na+ + CO32−
- CO32− + H2O ↔ HCO3− + OH−
Tác dụng với axit, tạo bọt và tạo muối, nước và khí cacbonic:
- Na2CO3 + 2HCl → 2NaCl + H2O + CO2
Tác dụng với muối tạo thành hai muối mới:
- Na2CO3 + CaCl2 → 2NaCl + CaCO3
Tác dụng với CO2 và nước xảy ra phản ứng thuận nghịch: Na2CO3 + CO2 + H2O ↔ 2NaHCO3
Tác dụng mạnh với F2, lithium, 2,4,6- trinitrotoluene.
Không tương thích với phosphorus peritoxit, fluoride, amonia + bạc nitrat, 2,4,6- trinitrotoluene, amonia, axit, natri sunfat + nước, hydrogen peroxit, nhôm (gây nổ khi nhôm đang nóng đỏ), natri sunfat, zic, canxi hidroxit, natri cacbonat + amonia (tạo thành dung dịch arabic gum gây nổ).
Các phương pháp sản xuất Natri cacbonat
Trong tự nhiên
Điều chế natri cacbonat: Natri cacbonat tồn tại trong tro của rong biển ở một số vùng biển phía Tây Nam Tây Ban Nha (25–30%) hoặc các hồ muối, mỏ muối dưới dạng Na2CO3.nH2O, Na2CO3.NaHCO3.2H2O ở những vùng thung lũng có nhiều mưa, không khí khô và gần núi vôi.
Xem thêm : Axit Salicylic Là Gì Và Những Thông Tin Quan Trọng Cần Biết
Điều chế natri cacbonat từ các loại đá quặng trong tự nhiên: Quặng natri cacbonat được tìm thấy nhiều nhất ở Botswana, Trung Quốc, Ai Cập, Ấn Độ, Kenia, Mêxicô, Pêru, Nam Phi, Thổ Nhĩ Kỳ và Mỹ. Trên thế giới có hơn 60 loại quặng natri cacbonat, chiếm 1/3 sản lượng natri cacbonat.
Tuy nhiên, việc thu nhận natri cacbonat thường không đạt độ tinh khiết cao do chứa nhiều tạp chất như muối clorua, sunfat và các chất không tan.
Hiện nay, có nhiều hồ, mỏ muối lớn chủ yếu ở châu Phi, châu Mỹ, châu Âu, Ấn Độ như Iagafdi, Bora, Tơ-ron, vùng Cát Biên, Segadin, Lu-na.

Để khai thác natri cacbonat từ lớp đất sâu, người ta đưa nước nóng vào giếng khoan để tan natri cacbonat cho đến khi nồng độ đạt 32 độ Bo-mê, sau đó đưa nước lên mặt đất và tiến hành quá trình tinh chế để thu được sản phẩm tinh khiết.
Trong công nghiệp
Điều chế na2co3: Phương pháp Leblanc, còn được gọi là phương pháp sunfat:
Nung hỗn hợp natri sunfat với than và đá vôi ở nhiệt độ 1000oC
- Na2SO4 + 2C → Na2S + 2CO2
- Na2S + CaCO3 → Na2CO3 + CaS
Hỗn hợp sản phẩm được hòa tan trong nước để tách CaS không tan. CaS có thể được sử dụng để sản xuất lưu huỳnh.
Phương pháp Solvay sử dụng amoniac:
- NaCl + NH3 + CO2 + H2O ↔ NaHCO3 + NH4Cl
Điều chế nahco3 từ na2co3:
NaHCO3 ít tan trong nước và được tách ra, sau đó nhiệt phân để tạo ra Na2CO3.
2NaHCO3 ↔ Na2CO3 + CO2 + H2O
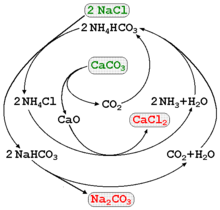
Các sản phẩm phụ sau phản ứng cũng có thể được sử dụng lại cho quá trình sản xuất Na2CO3 tiếp theo.
Cách làm natri cacbonat rất đơn giản và tôi đã từng thử áp dụng nó trong cuộc sống thực. Trong quá trình tìm hiểu về cách điều chế natri cacbonat, tôi đã tham khảo nhiều nguồn thông tin và thực hiện theo hướng dẫn. Tôi đã dùng các nguyên liệu có sẵn trong nhà như muối và baking soda, sau đó thực hiện quy trình pha chế để tạo natri cacbonat. Kết quả là tôi đã thành công, có được sản phẩm natri cacbonat chất lượng mà không tốn nhiều thời gian và công sức. Việc làm này thực sự tiết kiệm cho tôi khi cần sử dụng natri cacbonat trong các công việc hằng ngày như làm sạch hoặc pha chế đồ uống. Điều chế natri cacbonat tự tay mang lại niềm hứng thú và sự tiện lợi trong cuộc sống hàng ngày.
Những vai trò của Natri cacbonat
Xem thêm : Axit Bromhidric Hbr Là Gì – Những Thông Tin Cần Thiết Cho Bạn
Natri cacbonat – Na2CO3 có 2 dạng: dạng nặng và dạng nhẹ.
- Dạng nặng (khối lượng riêng là 1 kg/dm3): Được sử dụng trong công nghiệp chế tạo thủy tinh.
Natri cacbonat chiếm 13 – 15% tổng số nguyên liệu trong sản xuất thủy tinh. Nó được sử dụng để nấu thủy tinh, làm giảm nhiệt độ nung cát silic và tăng tính mềm dẻo. Dù chỉ chiếm vị trí thứ hai về khối lượng chất đưa vào, nhưng chi phí của nó lại chiếm tới 50 – 60% tổng chi phí nguyên liệu sản xuất.
- Dạng nhẹ (khối lượng riêng là 0,5 kg/dm3)
Trong công nghiệp sản xuất
- Trong ngành công nghiệp sản xuất các loại chất tẩy rửa, Natri cacbonat được sử dụng làm chất độn và chất phụ gia, chiếm khoảng 10 -12% sản lượng Na2CO3 trên toàn thế giới.

- Na2CO3 là chất đầu vào để sản xuất nhiều hợp chất của natri như xút ăn da, thủy tinh tan, cromat, dicromat, borac, chiếm đến 30% nhu cầu. Đôi khi, dung dịch Natri cacbonat lỏng còn được sử dụng thay thế cho Na2CO3.
- Dung dịch natri cacbonat được sử dụng để làm sạch lớp dầu mỡ trên bề mặt các chi tiết máy móc trước khi tiến hành phun sơn hoặc tráng kim loại.
- Nó cũng hỗ trợ loại bỏ lưu huỳnh trong xử lý nước thải và khí thải.
- Na2CO3 được sử dụng trong sản xuất cao su tổng hợp, chất nổ, tinh chế dầu.
Trong y tế
- Na2CO3 được sử dụng trong sản xuất một số loại thuốc sủi bọt như thuốc giảm đau đầu, bằng cách tạo bọt và tăng độ pH.
- Nó cũng được sử dụng trong sản xuất thuốc giảm đau dạ dày.
- Natri cacbonat có thể được dùng làm nước xúc miệng hoặc chà trực tiếp lên răng để loại bỏ mảng bám và làm trắng răng…

Trong công nghiệp thực phẩm
- Na2CO3 tinh khiết (bột nở) được sử dụng làm chất tạo xốp, giòn cho nhiều loại bánh như quẩy, muffin, cookies, bánh quy
- Ngoài ra, nó còn được sử dụng để làm giảm độ axit và chua của nước chanh, sốt cà chua.
- Na2CO3 có thể giúp rút ngắn thời gian nấu ăn và làm cho các loại đậu nhanh chín bằng cách ngâm chúng trong dung dịch Natri cacbonat. Việc này giúp giảm tình trạng đầy bụng sau khi ăn đậu.
- Natri cacbonat cũng làm mềm nhanh chóng các món hầm.

Theo tôi được biết, ca na2co3 có hơn 1500 ứng dụng khác nhau trong ngành công nghiệp, như sản xuất thủy tinh (chiếm khoảng 60% sản lượng sử dụng), chất chống ăn mòn, sản xuất xà bông, xi măng, sản xuất bột giặt và sản xuất chất làm mát.
Ở Việt Nam, nước ta nhập khẩu khoảng 120.000 tấn natri cacbonat mỗi năm để đáp ứng nhu cầu sản xuất trong các ngành công nghiệp khác nhau.
Mức độ nguy hiểm của Natri cacbonat
Đối với động vật
Gây chất độc cấp tính qua đường tiêu hóa LD50: 4090 mg/kg. Gây chất độc cấp tính qua đường hô hấp do bụi hóa chất LC50: 1200 mg/m3. Ảnh hưởng đến khả năng sinh sản.
Đối với con người
Tiếp xúc với da
- Tác động: Gây kích ứng da, làm hoại tử da, có thể gây ăn mòn tùy thuộc vào nồng độ, vị trí tiếp xúc và thời gian phơi nhiễm.
- Giải quyết: Dùng nước lạnh rửa kỹ vùng da tiếp xúc với hóa chất, lột bỏ quần áo đang mặc. Có thể sử dụng kem làm mềm da, xà phòng. Đưa nạn nhân đến bệnh viện gần nhất nếu có dấu hiệu bất thường.
Tiếp xúc với hệ hô hấp
- Tác động: Bụi hóa chất gây tổn thương trên đường hô hấp, niêm mạc mũi, lớp màng nhầy gây ra các triệu chứng ho, khó thở và có thể gây viêm phổi.
- Giải quyết: Đưa nạn nhân ra không gian thoáng đãng, tháo quần áo, cà vạt,… Nếu nạn nhân gặp khó thở, thậm chí ngừng thở, cần tiến hành hô hấp nhân tạo và đưa đến bệnh viện gần nhất.
Tiếp xúc với đường tiêu hóa
- Tác động: Gây tổn thương hệ tiêu hóa, gây kích ứng. Tùy thuộc vào nồng độ, nạn nhân có thể bị buồn nôn, nôn mửa, tiêu chảy, khát nước, đau bụng. Natri cacbonat hấp thụ vào máu cũng có tác hại đối với hệ tim mạch.
- Giải quyết: Nới lỏng quần áo nạn nhân đang mặc, thắt lưng, cà vạt,… Không gây nôn mửa cho nạn nhân trừ khi có nhân viên y tế hỗ trợ, không tiến hành hô hấp nhân tạo trực tiếp bằng miệng. Nếu nạn nhân nuốt quá nhiều hóa chất, cần đưa đến cấp cứu ngay lập tức.

Tiếp xúc với mắt
- Tác động: Gây tổn thương lớp niêm mạc mắt, khiến mắt bị phỏng, đỏ, sưng. Nếu natri cacbonat có nồng độ cao, đậm đặc, có thể gây mờ đục kính bảo vệ mắt mãi mãi.
- Giải quyết: Gỡ bỏ kính áp tròng nếu có thể. Dùng nước sạch rửa mắt nhiều lần trong ít nhất 15 phút, lựa chọn nước lạnh và nháy mắt. Đưa nạn nhân đến bác sĩ chuyên khoa mắt để kiểm tra và có phương pháp điều trị phù hợp.
Lưu ý:
- Khi sử dụng, cần đảm bảo sử dụng các trang thiết bị bảo hộ lao động như gang tay, quần áo, ủng, kính bảo hộ,… Nếu không có đủ không khí, cần sử dụng mặt nạ hô hấp có khả năng chống độc tốt.
- Trong trường hợp tràn đổ, rò rỉ hóa chất:
- Rò rỉ nhỏ: Dùng đất để phủ phần hóa chất rò rỉ, sau đó thu gom vào thùng chứa chất thải thích hợp. Phần cặn còn lại được xử lý bằng dung dịch axit axetic trước khi dùng nước để làm sạch.
- Rò rỉ lớn: Cố gắng thu gom nhiều hóa chất như có thể vào thùng chứa. Ngăn không cho hóa chất tràn ra nguồn nước, ống dẫn. Phần còn lại được xử lý như rò rỉ nhỏ. Nếu rò rỉ quá nhiều, hãy báo ngay cho cơ quan có thẩm quyền để có biện pháp xử lý.
- Bảo quản:
- Bảo quản trong khu vực khô ráo, thông thoáng không có các chất không tương thích. Các thùng, bao bì phải kín đáo và có mác cảnh báo nguy hiểm đầy đủ, tránh xa tầm tay trẻ em.
FAQ – Câu hỏi về điều chế natri cacbonat
Sự điều chế natri cacbonat là gì?
Điều chế natri cacbonat là quá trình sản xuất chất sodium carbonate từ nguyên liệu ban đầu chứa natri như soda, nước muối biển hoặc than đá. Thông qua một loạt các phản ứng hóa học, các nhà sản xuất có thể tạo ra sự phản ứng giữa natri và cacbonat để sản xuất natri cacbonat.
Sản phẩm natri cacbonat được sử dụng trong lĩnh vực nào?
Natri cacbonat có rất nhiều ứng dụng khác nhau. Trong ngành công nghiệp hóa chất, nó được sử dụng làm chất chống ăn mòn, chất làm sạch và chất ổn định. Trong ngành sản xuất thủy tinh, natri cacbonat giúp tạo ra kính và thủy tinh chất lượng cao. Ngoài ra, natri cacbonat cũng được sử dụng trong sản xuất xà bông, xi măng và thậm chí trong xử lý nước.
Sự điều chế natri cacbonat có ảnh hưởng đến môi trường không?
Quá trình sản xuất natri cacbonat cần sử dụng một số chất hóa học như muối, axit và nhiệt độ cao. Việc xử lý và tiêu thụ các chất thải này có thể gây ảnh hưởng tiêu cực đến môi trường nếu không được quản lý cẩn thận. Tuy nhiên, những nhà sản xuất có thể thực hiện các biện pháp xử lý chất thải và tái chế để giảm thiểu tác động tiêu cực này.

Hy vọng rằng bài viết trên đã giúp bạn hiểu rõ hơn về quá trình điều chế natri cacbonat và ứng dụng của nó trong ngành công nghiệp. Natri cacbonat có một loạt các ứng dụng quan trọng và không thể thiếu trong cuộc sống hàng ngày của chúng ta. Chúng ta cần nhận thức về tác động của quá trình sản xuất lên môi trường và khám phá các biện pháp xử lý chất thải để giảm thiểu ảnh hưởng tiêu cực. Hãy để lại nhận xét của bạn về bài viết này và chia sẻ nó với mọi người để lan tỏa kiến thức về điều chế natri cacbonat và tác động của nó!
Nguồn: https://oshovietnam.org
Danh mục: Giáo Dục







Leave a Reply